L'entreprise intensifie les préparatifs de commercialisation de la plateforme spécifique à son « dispositif révolutionnaire »
MINNEAPOLIS--(BUSINESS WIRE)--HistoSonics® (www.histosonics.com), qui produit le système Edison® et les nouvelles plateformes de traitement par histotripsie, a annoncé aujourd'hui avoir reçu l'autorisation de commercialisation de sa plateforme « révolutionnaire » de la part de la US Food and Drug Administration (FDA) à l'issue d'une demande de classification De Novo, soit un rigoureux mécanisme d'évaluation préalable à la mise sur le marché et destiné aux dispositifs médicaux sans aucun prédicat existant. Cette autorisation de commercialisation fait d'Edison la première et unique plateforme d'histotripsie disponible aux États-Unis.


La FDA a en partie accordé son autorisation sur la base des données issues des essais #HOPE4LIVER réalisés sur 13 sites en Europe et aux États-Unis. Les données obtenues lors des essais menés en Europe/au Royaume-Uni et aux États-Unis ont été regroupées et utilisées pour évaluer l'innocuité et l'efficacité cliniques de l'histotripsie lorsqu'elle est pratiquée pour détruire des tumeurs hépatiques primaires et secondaires ciblées. En examinant ces données conjointement, on a constaté que l'histotripsie avait permis de remplir les principaux critères d'efficacité et d'innocuité, et ce, après évaluation de l'innocuité chez 44 sujets et évaluation de l'efficacité du traitement sur 44 tumeurs. Un des aspects valant la peine d'être noté est l'hétérogénéité des sujets traités : 18 présentant des carcinomes hépatocellulaires (CHC) et 26 présentant des tumeurs métastatiques du foie dont l'origine primaire était le colon, le rectum, le sein ou autres. Comme en a récemment fait état une présentation lors du congrès annuel de la CIRSE (Société européenne de radiologie cardiovasculaire et interventionnelle) à Copenhague, un taux de réussite technique de 95,5 % a été atteint, ce qui signifie que les médecins sont capables de cibler avec précision et de détruire des tissus et des tumeurs non résécables du foie. Par ailleurs, seuls trois événements indésirables de niveau 3 ou plus selon la classification CTCAE ont été observés parmi les 44 sujets traités au cours des 30 jours ayant suivi l'histotripsie, ce qui représente un taux de complication de 6,8 %, ces effets étant non spécifiques à l'histotripsie et fréquents lors des thérapies focales classiques.
« Il s'agit du cap le plus important franchi par HistoSonics à ce jour. Cela représente plus de deux décennies de travail acharné, de la création du système à l'université du Michigan en 2001 – que l'on avait toujours considérée comme impossible – à la maîtrise des nombreuses complexités de l'histotripsie et à l'intégration de celle-ci sous forme de plateforme clinique totalement non invasive », a expliqué Mike Blue, président et PDG d'HistoSonics. L'entreprise a déclaré avoir élargi ses capacités commerciales et opérationnelles par rapport à l'année précédente pour se préparer à la commercialisation. Et M. Blue d'ajouter : « Nous nous sommes judicieusement entourés de professionnels ayant une vaste expérience dans le domaine opérationnel, de l'éducation et du développement de marché, et nous sommes prêts à entamer la planification des formations des médecins immédiatement. C'est un jour fantastique pour les patients qui profiteront des avantages révolutionnaires de l'histotripsie et je félicite la FDA d'avoir travaillé si diligemment avec nous tout au long du processus d'évaluation. »
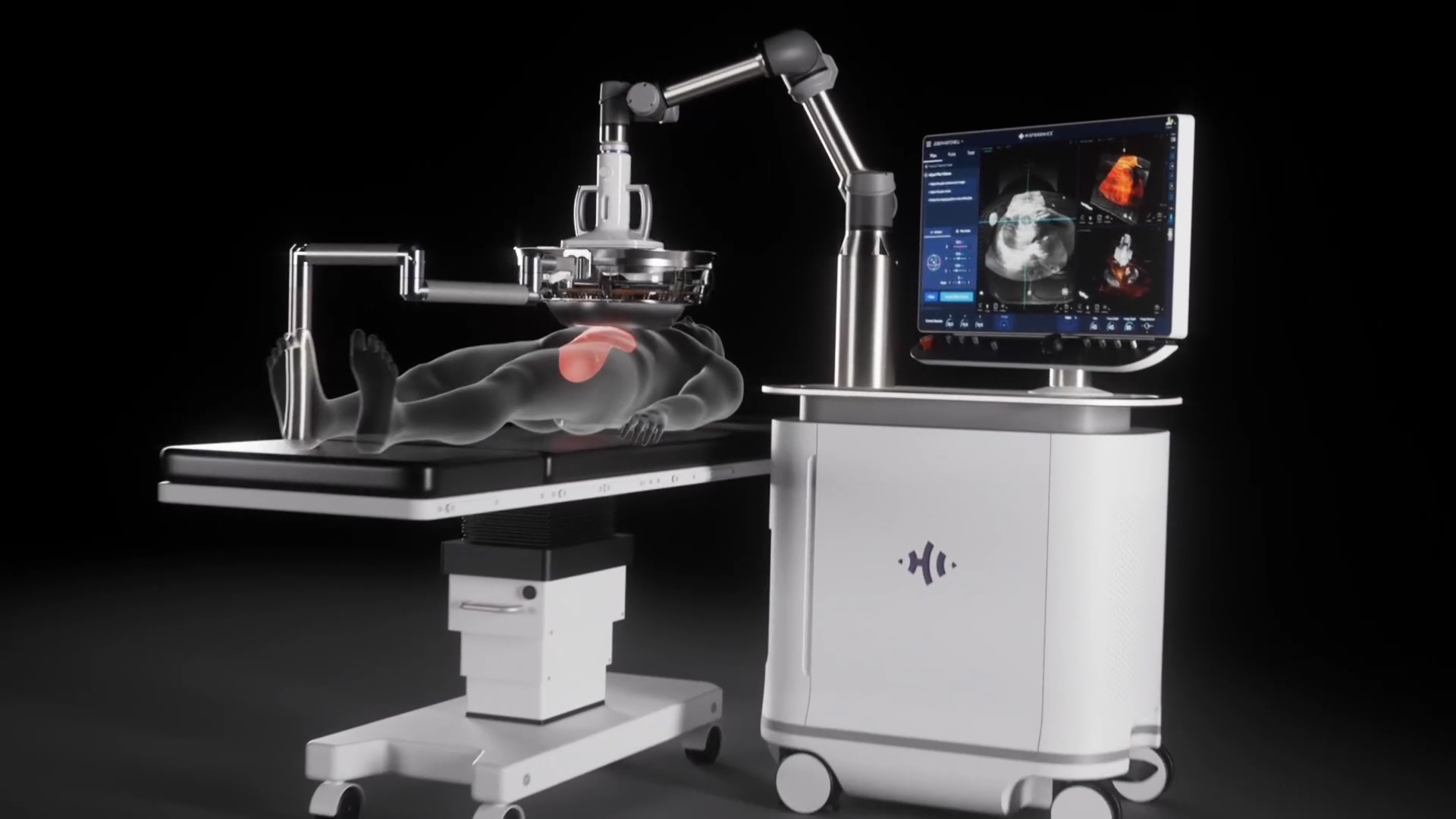
La science de l'histotripsie exploite une énergie sonore focalisée pour générer une cavitation acoustique contrôlée qui liquéfie et détruit mécaniquement les tissus hépatiques ciblés aux niveaux subcellulaires, y compris les tumeurs. Le système Edison d'HistoSonics a recours à des techniques d'imagerie avancées et à une technologie exclusive pour proposer, avec maîtrise et précision, des traitements par histotripsie non invasifs et personnalisés. L'entreprise pense que le nouveau mécanisme d'action de sa technologie exclusive pourrait offrir d'importants avantages aux patients, notamment la guérison et la résorption rapides de l'organe traité. Plus spécifiquement, la plateforme d'HistoSonics permet également aux médecins de surveiller la destruction des tissus grâce à une visualisation et à un contrôle continus en temps réel, chose qu'aucun autre dispositif ne permet de faire à l'heure actuelle.
« Pour un chirurgien, il est gratifiant d'être en mesure de proposer une procédure donnant la possibilité de détruire avec précision des tumeurs hépatiques sans utiliser de scalpels ni d'aiguilles, ce qui devrait permettre au patient de guérir rapidement tout en évitant certaines complications liées aux infections du champ opératoire ou aux irradiations causées par d'autres méthodes », a indiqué le Dr Joe Amaral, vice-président des affaires médicales d'HistoSonics. « Vu les données et les expériences menées sur les patients lors de nos études, nous sommes convaincus que l'histotripsie aura un impact significatif sur les patients atteints de maladies hépatiques non résécables, y compris des tumeurs. Nous avons hâte de voir quel rôle jouera l'histotripsie dans les futures stratégies thérapeutiques », a déclaré le Dr Amaral.
Le système Edison vise l'ablation non invasive des tumeurs hépatiques, y compris les tumeurs hépatiques non résécables, au moyen d'un procédé mécanique et non thermique basé sur les ultrasons focalisés.
À propos d'HistoSonics
HistoSonics est une société privée de dispositifs médicaux ayant mis au point une thérapie exclusive par faisceau sonique et une plateforme non invasive basées sur la science de l'histotripsie, un mécanisme d'action innovant qui a recours à des ultrasons focalisés pour liquéfier et détruire mécaniquement des tumeurs et des tissus indésirables. L'entreprise concentre actuellement ses efforts sur la commercialisation de son système de traitement hépatique Edison aux États-Unis et sur certains marchés mondiaux spécifiques tout en élargissant les applications de l'histotripsie à d'autres organes comme les reins, le pancréas, etc. HistoSonics possède des bureaux à Ann Arbor dans le Michigan et à Minneapolis dans le Minnesota.
Pour obtenir de plus amples informations, rendez-vous sur : www.histosonics.com/.
Le texte du communiqué issu d’une traduction ne doit d’aucune manière être considéré comme officiel. La seule version du communiqué qui fasse foi est celle du communiqué dans sa langue d’origine. La traduction devra toujours être confrontée au texte source, qui fera jurisprudence.
Contacts
Contact de presse :
Josh King
Vice-président du marketing
E-mail : Joshua.king@histosonics.com
Téléphone : 608.332.8124